О методе
История вопроса
Брахитерапия считается реальной альтернативой радикальной простатэктомии и дистанционной лучевой терапии, и возможно полное излечение заболевания рака предстательной железы при правильном подборе больных и профессиональном выполнении операции.
Впервые брахитерапия была применена в 1910 году, когда Д. Пасто и П. Дегрэ ввели капсулы радия-226 в предстательную железу через уретру.
Далее в 1917 году в США Б. Барринджер ввел микроисточники в железу через иглы. Затем Р. Флокс вместе с соавторами в 1930 году применили в качестве имплантанта радиоактивное золото.

Возрождение брахитерапии рака предстательной железы началось в 1970 году с развитием технологии ретропубикальной открытой имплантации зерен I-125 в Мемориальном Госпитале Нью-Йорка. Однако, при открытой ретропубикальной технологии зерна йода располагались мануально, вследствие чего не достигалось оптимального распределения дозы в предстательной железе: наряду с зонами чрезмерной активности оставались холодные очаги.
В 1981 году Х. Холм и Дж. Гаммелгард применили технологию имплантации микроисточников йода-125 в ткань предстательной железы под контролем трансректального ультразвукового сканирования (ТРУЗИ). Это методика впервые была применена для получения биопсии, и стало очевидным, что она может использоваться для визуализации положения радиоактивных источников в простате. Это и послужило основой новой технологии брахитерапии.
В 1990 году П. Кутревелис использовал трехмерную стереотактическую приставку к компьютерному томографу (КТ) для лечения больных раком предстательной железы, которым невозможно провести лечение методом брахитерапии под контролем ТРУЗИ.
В 2000 году в НИИ урологии Минздрава России г. Москвы был внедрен новый метод лечения рака предстательной железы – брахитерапия. Этот институт стал первым медицинским учреждением в России, который освоил брахитерапию – уникальную технологию, известную и применяемую во всем мире.
С 2004 года метод профессора П. Кутревелиса (проведение брахитерапии под контролем КТ) используется в Центре брахитерапии в Медицинском Радиологическом Научном Центре РАМН г. Обнинска.
Метод Брахитерапии
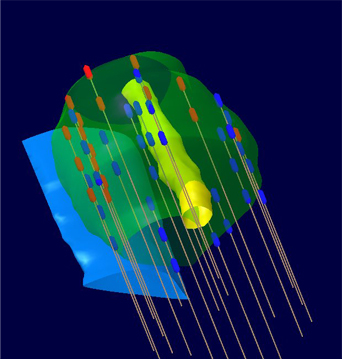
При выявлении рака предстательной железы на стадии T1 – Т2 (в некоторых случаях и на стадии Т3) наряду с радикальной простатэктомией и дистанционной гамма-терапией может быть применен менее травматичный и новый метод лечения данного заболевания – БРАХИТЕРАПИЯ.
Брахитерапия (от греч. слова “brachios” – короткий, быстрый) – это современный и высокотехнологичный метод лечения рака предстательной железы, когда микроисточники радиоактивного излучения на основе I-125 вводятся внутрь пораженного органа.
При этом максимальная доза излучения доставляется непосредственно в опухоль без поражения прилегающих органов и тканей. В простату под контролем ультразвукового аппарата (или под контролем КТ – компьютерного томографа) специальными иглами вводят небольшие, меньше рисового зернышка, металлические капсулы с радиоактивным йодом, которые постепенно губят раковые клетки.
Каждое зернышко облучает очень маленькое пространство, поэтому прилегающие здоровые ткани и органы не подвергаются повреждению. Считается, что брахитерапия – наиболее щадящий на сегодняшний день метод лечения.
Этапы операции
1. Подготовка к операции
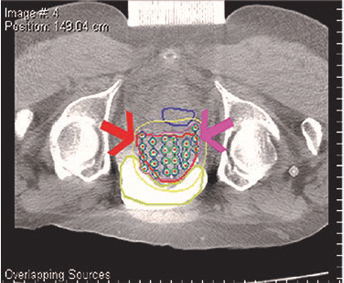
Первый этап подготовительный, в ходе которого проводится предимплантационное исследование пациента (обычно за 3-4 недели до операции) на мульти-спиральном компьютерном томографе, либо с помощью трансректального ультразвукового датчика. На основании полученных данных анализируется состояние и размеры предстательной железы, и семенных пузырьков. Возможно, после анализа полученных изображений, урологом будет принято решение о проведении биопсии семенных пузырьков с целью уточнения стадии заболевания и распространения злокачественных клеток. Полученные и проанализированные снимки передаются в компьютерную систему планирования лучевой терапии, где выполняется трехмерная объемная реконструкция анатомических структур: предстательной железы, семенных пузырьков, уретры, прямой кишки и мочевого пузыря.
Это необходимо, чтобы при предоперационной дозиметрии достоверно оценить лучевую нагрузку на все органы. Затем проводится предварительное планирование расположения источников и анализ дозного распределения. Главная цель – достижение равномерной дозы радиации в предстательной железе.
Дозиметрическое планирование
На полученных изображениях врач-уролог производит оконтуривание предстательной железы, уретры и прямой кишки.
Расчет доз осуществляется с помощью специальной компьютерной программы. Этот этап выполняет медицинский физик. Полученные изображения с контурами предстательной железы, уретры и прямой кишки импортируются в компьютерную планирующую систему. Зерна располагаются в узлах координатной сетки в соответствии с необходимой дозой излучения.
СОД очаговая доза рассчитывается на весь срок 596 суток активной персистенции импланта и составляет 160 Гр в предстательной железе. Нижний предел эффективной дозы составляет 144 Гр по контуру предстательной железы. При этом максимальная допустимая нагрузка на уретру составляет 140 Гр, прямая кишка и мочевой пузырь 30 Гр, причем не должна превышать 30% от объема, рассчитанного при планировании, обычно 1-1,5 см3 . Использование низких энергий гарантирует высокий градиент падения дозы. Нагрузка на прочие органы и структуры малого таза не превышает 0,1 Гр. Адекватность дозиметрического плана и доз оценивается лучевым терапевтом.
Существуют разные подходы к распределению зерен в разных центрах. Однако общим является расчет дозы, основанной на анатомии каждой индивидуальной предстательной железы, а не на принятом стандарте.
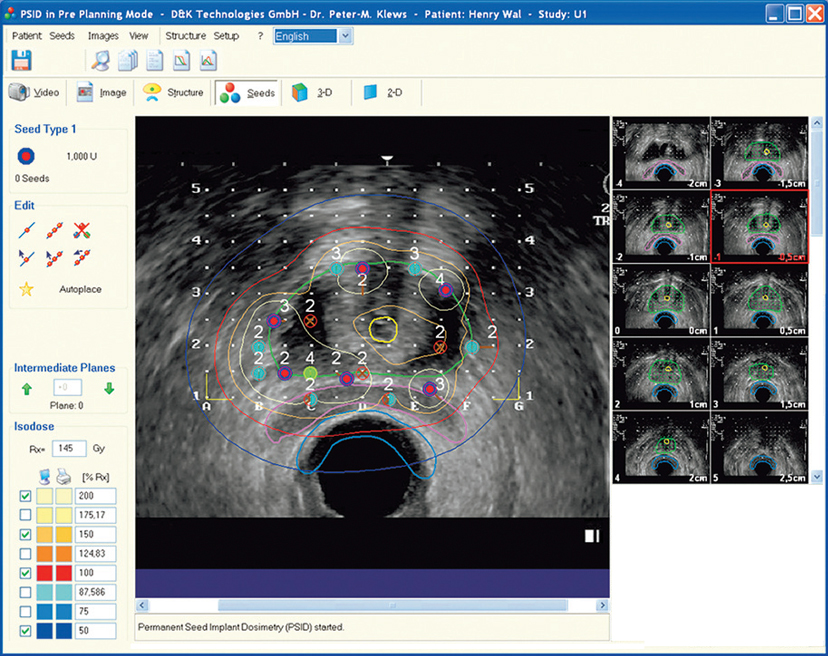
PSID 4.1.2 - программа планирования брахитерапии
Таким образом, подбирается наиболее оптимальная терапия с учетом индивидуальных особенностей каждого пациента. Благодаря тому, что микроисточники вводятся в предстательную железу, возможно увеличение дозы излучения в 2-3 раза по сравнению с дистанционной лучевой терапией, а с увеличением дозы излучения растут шансы излечения. Общепринятой дозой при имплантации изотопов радиоактивного йода (I-125) является величина в 140-160 Грей.
Подготовка микроисточников к операции

источник представляет собой цилиндрическую титановую микрокапсулу, внутри которой находятся изотопы радиоактивного I-125
В соответствии с ранее подобранным дозиметрическим планом, через специальный шаблон в предстательную железу вводятся иглы, которые доставят источники в ткань. Шаг шаблона – 2.5 мм. Столь маленький шаг позволяет добиться высокой точности расположения микрокапсул.

2. Процедура имплантации
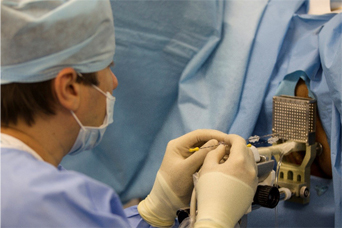
Второй этап – это непосредственно сама процедура имплантации источников в предстательную железу и в семенные пузырьки (в случае их поражения опухолевыми клетками).
Имплантируемый в ткань предстательной железы источник представляет собой цилиндрическую титановую микрокапсулу, внутри которой находятся изотопы радиоактивного I-125. Источники (“зерна”) закреплены на специальной нити, которая позволяет зафиксировать местоположение капсул в предстательной железе и исключить риск их свободного перемещения.
Имплантация микроисточников под ультразвуковым контролем
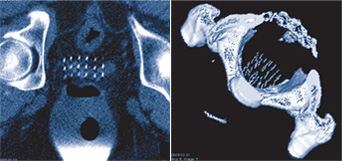
Имплантация радиоактивных “зерен” проводится в операционной под местным наркозом и длится около 2 часов. Ультразвуковой датчик вводится в прямую кишку для получения изображения предстательной железы на телевизионном мониторе. Зерна, содержащие йод-125 и фиксированные на нити (обычно в количестве 60-90 в зависимости от определенного объема железы), доставляются в предстательную железу закрытым способом через иглы, которые вводятся через кожу промежности между мошонкой и прямой кишкой. Положение игл и зерен контролируется на экране монитора.
Источники (“зерна”) закреплены на специальной нити, которая позволяет зафиксировать местоположение капсул в предстательной железе и исключить риск их свободного перемещения.
Положение игл и зерен контролируется на экране монитора.
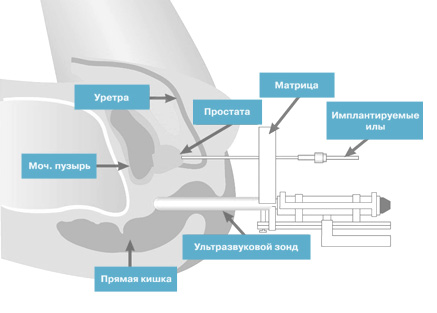
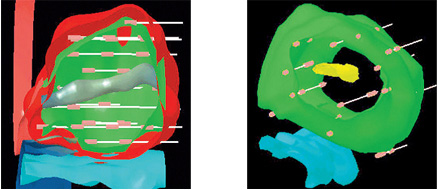
Имплантация микроисточников под контролем трехмерной стереотактической приставки к спиральному компьютерному томографу
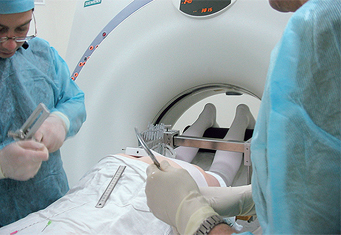
Вся процедура имплантации радиоактивных микроисточников производится под эпидуральным наркозом (в некоторых случаях применяется общий наркоз), который действуeт на нижнюю часть тела. В течение процедуры, продолжительностью 1-2 часа, на компьютерном томографе проводится постоянный мониторинг хода операции, который позволяет в режиме реального времени контролировать процесс введения источников.
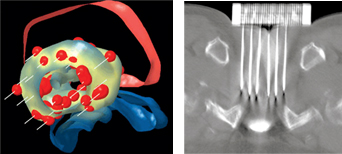
Поскольку зерна доставляются непосредственно в простату, концентрация излучения внутри опухоли в 2-3 раза выше, чем при дистанционной лучевой терапии, где используются более низкие дозы из-за опасения повредить здоровые ткани. Источник герметичен, поэтому облучения медицинского персонала практически не происходит, и нет необходимости в специальном обустройстве палат, канализации и других повышенных мерах радиационной безопасности.
По окончании процедуры в мочевой пузырь временно помещается катетер для эвакуации мочи. После удаления игл зерна остаются в простате и обеспечивают нужный уровень радиоактивного излучения в течение нескольких недель. Йод-125 имеет период полураспада 60 дней, обычно рекомендованная минимальная периферическая доза составляет 140-160 Грей.
3. После операции

Третий этап – постимплантационная дозиметрия и общий контроль расположения источников. На этом этапе проводится оценка лучевой нагрузки на пораженную ткань и, так называемые, “органы риска”: мочевой пузырь, уретру и прямую кишку. Максимальное поражение опухолевой ткани при максимальном сохранении здоровых тканей – одно из главных условий, определяющих эффективность брахитерапии. Для каждого органа строится гистограмма доза-объем, которая позволяет проанализировать полученную дозу. Через 4-6 недель после операции на компьютерном томографе проводится дополнительный контроль расположения источников.
На всех этапах проведения брахитерапии с пациентом работает команда специалистов, в составе которой врач-уролог, врач-диагност и медицинский физик. Все специалисты проходят обучение за границей и имеют соответствующиесертификаты. Кроме того, после имплантации больной помещается в после-операционную палату. В мочевой пузырь устанавливается катетер, который обычно убирают на следующий день, после чего пациент может выписаться домой. Принимать пищу можно сразу после процедуры.
Следует избегать физических нагрузок в течение первых двух дней, после этого пациент может возвратиться к своей обычной деятельности.
Метод брахитерапии считается малоинвазивным, то есть малоповреждающим. Пациенты переносят его хорошо. На следующий день после радиоактивных “инъекций” больного выписывают, через неделю он уже может работать, а через пару месяцев забудет о своих проблемах. Процент выздоровления после подобной процедуры высокий, сравнимый с радикальной простатэктомией. Осложнения если и возникают, то гораздо меньше, чем те, что развиваются при обычном лечении.
Преимущества
-
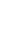 Доказанная эффективность
Доказанная эффективностьМногочисленные клинические исследования показали, что брахитерапия рака предстательной железы является эффективным лечением рака предстательной железы. При ее применении вероятность излечения достигает 90%.
-
 Минимальные побочные эффекты
Минимальные побочные эффектыТочность и направленность низкодозной брахитерапии сокращает риск побочных эффектов, таких как недержание мочи и эректильная дисфункция.
-
 Минимальная инвазивность и короткий период восстановления
Минимальная инвазивность и короткий период восстановленияДля брахитерапии не требуется обширная операция. Период восстановления после брахитерапии меньше, чем после операции (дни по сравнению с неделями).
-
 Небольшая длительность операции
Небольшая длительность операцииПроцедура выполняется амбулаторно и пребывание в клинике ограничивается одними сутками. Большинство пациентов могут возвращаться к выполнению обычной работы на следующий день после имплантации.
-
 Приемлемость для пациентов
Приемлемость для пациентовБрахитерапия может быть применима к пациентам, которым не показано радикальное хирургическое лечение, а также у больных, которым противопоказана наружная лучевая терапия вследствие наличия патологии кишечника внутри полей радиации, особенно у пациентов с воспалительными заболеваниями. Кроме того, данная процедура хорошо переносится пациентами с тяжелыми сопутствующими заболеваниями, а также пожилыми людьми.
-
 Лечение для граждан РФ проводится бесплатно более чем в 30 клиниках по всей России.
Лечение для граждан РФ проводится бесплатно более чем в 30 клиниках по всей России.Операции низкодозной брахитерапии выполняются в России, начиная с 2004 года, и входят в перечень высокотехнологичной медицинской помощи (ВМП), оплачиваемой за счет государства. Метод успешно применяют 30 государственных медицинских центров по всей России. Пролечено более 8000 пациентов.
Видео операции
-
Интервью с председателем правления Объединения Брахитерапевтов России Свиридовым Павлом Владимировичем о низкодозной брахитерапии
-
Видео операции Видео реальной операции в клинике города Москвы, проведенную Ивановым Иваном Алексеевичем Операция длилась 3 часа 15 минут.
Клиники
-
Брахитерапия рака предстательной железы (рака простаты) в городе Москва:
КЛИНИЧЕСКИЙ ЦЕНТР ПМГМУ ИМЕНИ И.М.СЕЧЕНОВА sechenovclinic.ru
ГБНУ «РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ НАУЧНЫЙ ЦЕНТР ИМЕНИ Н.Н. БЛОХИНА» РАМН www.ronc.ru
ФГБУ "РОССИЙСКИЙ НАУЧНЫЙ ЦЕНТР РЕНТГЕНОРАДИОЛОГИИ" www.rncrr.ru
ФГБУ "НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ УРОЛОГИИ ИМ. Н.А. ЛОПАТКИНА" - ФИЛИАЛ "ФЕДЕРАЛЬНОГО МЕДИЦИНСКОГО ИССЛЕДОВАТЕЛЬСКОГО ЦЕНТРА ИМ. П.А. ГЕРЦЕНА" МИНЗДРАВА РОССИИ uroline.nmicr.ru
ФГБУ ГОСУДАРСТВЕННЫЙ НАУЧНЫЙ ЦЕНТР РФ «ФЕДЕРАЛЬНЫЙ МЕДИЦИНСКИЙ БИОФИЗИЧЕСКИЙ ЦЕНТР ИМЕНИ А.И. БУРНАЗЯНА» ФМБА РОССИИ fmbafmbc.ru
ГБУЗ "ГОРОДСКАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА ИМЕНИ С.И. СПАСОКУКОЦКОГО (ГКБ № 50)" 50gkb.ru
ГБУЗ "ГОРОДСКАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА ИМЕНИ Д.Д. ПЛЕТНЕВА (ГКБ № 57)" gkb57.ru
ГБУЗ "ГОРОДСКАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА ИМЕНИ С.П. БОТКИНА" botkinmoscow.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Екатеринбург:
ГБУЗ СО "СВЕРДЛОВСКАЯ ОБЛАСТНАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА №1 www.okb1.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Иркутск:
ГБУЗ "ОБЛАСТНОЙ ОНКОЛОГИЧЕСКИЙ ДИСПАНСЕР" irkood.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Казань:
РЕСПУБЛИКАНСКИЙ КЛИНИЧЕСКИЙ ОНКОЛОГИЧЕСКИЙ ДИСПАНСЕР МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ ТАТАРСТАН oncort.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Красноярск:
ФГБУЗ "СИБИРСКИЙ КЛИНИЧЕСКИЙ ЦЕНТР" ФМБА РОССИИ www.skc-fmba.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Нижний Новгород:
ФБУЗ "ПРИВОЛЖСКИЙ ОКРУЖНОЙ МЕДИЦИНСКИЙ ЦЕНТР" ФМБА РОССИИ www.pomc.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Новосибирск:
ФГБУ "НОВОСИБИРСКИЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ПАТОЛОГИИ КРОВООБРАЩЕНИЯ ИМЕНИ АКАДЕМИКА Е.А. МЕШАЛКИНА" МИНЗДРАВА РОССИИ meshalkin.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Обнинск:
ФГБУ "МЕДИЦИНСКИЙ РАДИОЛОГИЧЕСКИЙ НАУЧНЫЙ ЦЕНТР ИМ. А.Ф. ЦЫБА - ФИЛИАЛ ФГБУ "ФЕДЕРАЛЬНОГО МЕДИЦИНСКОГО ИССЛЕДОВАТЕЛЬСКОГО ЦЕНТРА ИМ. П.А. ГЕРЦЕНА" МИНЗДРАВА РОССИИ mrrc.nmicr.ru
ФГБУЗ КБ №8 ФМБА РОССИИ www.кб8.рф
-
Брахитерапия рака предстательной железы (рака простаты) в городе Ростов-на-Дону:
ФГБУ "РОСТОВСКИЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ОНКОЛОГИЧЕСКИЙ ИНСТИТУТ" МИНЗДРАВА РОССИИ www.rnioi.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Самара:
ГБУЗ "САМАРСКИЙ ОБЛАСТНОЙ КЛИНИЧЕСКИЙ ОНКОЛОГИЧЕСКИЙ ДИСПАНСЕР" samaraonko.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Санкт-Петербург:
ФГБУЗ "КЛИНИЧЕСКАЯ БОЛЬНИЦА № 122 ИМ. Л.Г. СОКОЛОВА" ФМБА РОССИИ med122.com
-
Брахитерапия рака предстательной железы (рака простаты) в городе Тюмень:
ОАО "МЕДИКО-САНИТАРНАЯ ЧАСТЬ НЕФТЯНИК" www.clinica72.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Уфа:
КЛИНИКА ГБОУ ВПО "БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ" kbgmu.ru
ГБУЗ "РЕСПУБЛИКАНСКИЙ КЛИНИЧЕСКИЙ ОНКОЛОГИЧЕСКИЙ ДИСПАНСЕР" onkorb.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Химки:
ФГБУ "ФЕДЕРАЛЬНЫЙ КЛИНИЧЕСКИЙ ЦЕНТР ВЫСОКИХ МЕДИЦИНСКИХ ТЕХНОЛОГИЙ" ФМБА РОССИИ www.kb119.ru
-
Брахитерапия рака предстательной железы (рака простаты) в городе Челябинск:
ГБУЗ "ЧЕЛЯБИНСКИЙ ОКРУЖНОЙ КЛИНИЧЕСКИЙ ОНКОЛОГИЧЕСКИЙ ДИСПАНСЕР" www.chelonco.ru
Стоимость проведения лечения
Лечение рака методом низкодозной брахитерапии включено в перечень высокотехнологичной медицинской помощи (ВМП) гражданам РФ.
В России низкодозная брахитерапия внесена в перечень видов высокотехнологической медицинской помощи, финансируемой в том числе, за счет государства в рамках программы государственных гарантий бесплатного оказания медицинской помощи. Пациенту лечение рака предстательной железы методом низкодозной брахитерапии предоставляется бесплатно.
Что такое квота на ВМП?
Высокотехнологичная медицинская помощь (ВМП) – это медицинская помощь с применением высоких медицинских технологий для лечения сложных заболеваний. ВМП оказывается в профильных лечебных учреждениях, которые имеют лицензию на оказание данного вида помощи.
Как получить квоту на ВМП?
Подробнее о получении высокотехнологичной медицинской помощи (ВМП) можно прочитать на официальном сайте Федерального Фонда обязательного медицинского страхования: http://www.ffoms.ru/for-citizens/about-oms/#high-tech-help

